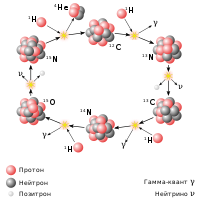
Изотопы
Изото́пы (от др.-греч. ἴσος «равный; одинаковый» + τόπος «место») — разновидности атомов (и ядер) химического элемента, имеющие одинаковый атомный номер, но разные массовые числа[1]. Название связано с тем, что все изотопы одного атома помещаются в одно и то же место (в одну клетку) таблицы Менделеева[2]. Химические свойства атома зависят от строения электронной оболочки, которая, в свою очередь, определяется в основном зарядом ядра Z (то есть количеством протонов в нём), и почти не зависят от его массового числа A (то есть суммарного числа протонов Z и нейтронов N).
Все изотопы одного элемента имеют одинаковый заряд ядра, различаясь лишь числом нейтронов. Обычно изотоп обозначается символом химического элемента, к которому он относится, с добавлением верхнего левого индекса, означающего массовое число (например, 12C, 222Rn). Можно также написать название элемента с добавлением через дефис массового числа (например, углерод-12, радон-222)[3]. Некоторые изотопы имеют традиционные собственные названия (например, дейтерий, актинон).
Различают изотопы устойчивые (стабильные) и радиоактивные[4]. На 2017 год было известно 3437 изотопов всех элементов, из них 252 изотопа стабильны[5].
Пример изотопов: 16
8O, 17
8O, 18
8O — три стабильных изотопа кислорода.
Терминология[править | править код]
Первоначально изотопы также назывались изотопными элементами[6], а в настоящее время иногда называют изотопными нуклидами[7].
Основная позиция ИЮПАК состоит в том, что правильным термином в единственном числе для обозначения атомов одного химического элемента с одинаковой атомной массой является нуклид, а термин изотопы допускается применять для обозначения совокупности нуклидов одного элемента. Термин изотопы был предложен и применялся изначально во множественном числе, поскольку для сравнения необходимо минимум две разновидности атомов. В дальнейшем в практику широко вошло также употребление термина в единственном числе — изотоп. Кроме того, термин во множественном числе часто применяется для обозначения любой совокупности нуклидов, а не только одного элемента, что также некорректно. В настоящее время позиции международных научных организаций не приведены к единообразию и термин изотоп продолжает широко применяться, в том числе и в официальных материалах различных подразделений ИЮПАК и ИЮПАП. Это один из примеров того, как смысл термина, изначально в него заложенный, перестаёт соответствовать понятию, для обозначения которого этот термин используется (другой хрестоматийный пример — атом, который, в противоречии с названием, не является неделимым).
История открытия изотопов[править | править код]
Первое доказательство того, что вещества, имеющие одинаковое химическое поведение, могут иметь различные физические свойства, было получено при исследовании радиоактивных превращений атомов тяжёлых элементов. В 1906—1907 годах выяснилось, что продукт радиоактивного распада урана — ионий и продукт радиоактивного распада тория — радиоторий имеют те же химические свойства, что и торий, но отличаются от него атомной массой и характеристиками радиоактивного распада. Было обнаружено позднее, что у всех трёх продуктов одинаковы оптические и рентгеновские спектры. Такие вещества, идентичные по химическим свойствам, но различные по массе атомов и некоторым физическим свойствам, по предложению английского учёного Содди с 1910 г. стали называть изотопами[источник не указан 1069 дней].
На март 2017 года известно 3437 изотопов всех элементов[5], из них 254 стабильных, 29 условно-стабильных (с периодом полураспада более 10 миллиардов лет), 294 (9 %) изотопы трансурановых элементов, 1209 (38 %) нейтронно-избыточных и 1277 (40 %) протонно-избыточных (то есть отклоняющихся от линии бета-стабильности в сторону избытка нейтронов или протонов, соответственно). По количеству открытых изотопов первое место занимают США (1237), затем идут Германия (558), Великобритания (299), СССР/Россия (247) и Франция (217). Среди лабораторий мира первые пять мест по числу открытых изотопов занимают Национальная лаборатория им. Лоуренса в Беркли (638), Институт тяжёлых ионов в Дармштадте (438), Объединённый институт ядерных исследований в Дубне (221), Кавендишская лаборатория в Кембридже (218) и ЦЕРН (115). За 10 лет (2006—2015 годы включительно) в среднем физики открывали в год 23 нейтронно-избыточных и 3 протонно-избыточных изотопа, а также 4 изотопа трансурановых элементов. Общее количество учёных, являвшихся авторами или соавторами открытия какого-либо изотопа, составляет 3598 человек[8][9].
Изотопы в природе[править | править код]
Известно, что изотопный состав большинства элементов на Земле одинаков во всех материалах. Некоторые физические процессы в природе приводят к нарушению изотопного состава элементов (природное фракционирование изотопов, характерное для лёгких элементов, а также изотопные сдвиги при распаде природных долгоживущих изотопов). Постепенное накопление в минералах ядер — продуктов распада некоторых долгоживущих нуклидов используется в ядерной геохронологии.
Особое значение имеют процессы образования изотопов углерода в верхних слоях атмосферы под воздействием космического излучения. Эти изотопы распределяются в атмосфере и гидросфере планеты, вовлекаются в оборот углерода живыми существами (животными и растениями). Изучение распределения изотопов углерода лежит в основе радиоуглеродного анализа.
Применение изотопов человеком[править | править код]
В технологической деятельности люди научились изменять изотопный состав элементов для получения каких-либо специфических свойств материалов. Например, 235U способен к цепной реакции деления тепловыми нейтронами и может использоваться в качестве топлива для ядерных реакторов или ядерного оружия. Однако в природном уране лишь 0,72 % этого нуклида, тогда как цепная реакция практически осуществима лишь при содержании 235U не менее 3 %. В связи с близостью физико-химических свойств изотопов тяжёлых элементов процедура изотопного обогащения урана является крайне сложной технологической задачей, которая доступна лишь десятку государств в мире. Во многих отраслях науки и техники (например, в радиоиммунном анализе) используются изотопные метки.
Нуклиды 60Co и 137Cs используются в стерилизации γ-лучами (лучевая стерилизация) как один из методов физической стерилизации инструментов, перевязочного материала и прочего. Доза проникающей радиации должна быть весьма значительной — до 20-25 кГр, что требует особых мер безопасности. В связи с этим лучевая стерилизация проводится в специальных помещениях и является заводским методом стерилизации (непосредственно в стационарах она не производится).[10]
| Количество энергетических уровней электронной оболочки |
Количество протонов (электронов) |
Символ | Элемент | Количество протонов и нейтронов |
Изотопная распространённость на Земле, % |
|---|---|---|---|---|---|
| 1 | 1 | H | Водород | 1 2 |
99,98 0,02 |
| 1 | 2 | He | Гелий | 3 4 |
0,00001 99,99999 |
| 2 | 3 | Li | Литий | 6 7 |
7,9 92,1 |
| 2 | 4 | Be | Бериллий | 9 | 100 |
| 2 | 5 | B | Бор | 10 11 |
18,8 81,2 |
| 2 | 6 | C | Углерод | 12 13 |
98,9 1,1 |
| 2 | 7 | N | Азот | 14 15 |
99,62 0,38 |
| 2 | 8 | O | Кислород | 16 17 18 |
99,76 0,04 0,20 |
| 2 | 9 | F | Фтор | 19 | 100 |
| 2 | 10 | Ne | Неон | 20 21 22 |
90,48 0,27 9,25 |
| 3 | 11 | Na | Натрий | 23 | 100 |
| 3 | 12 | Mg | Магний | 24 25 26 |
78,6 10,1 11,3 |
| 3 | 13 | Al | Алюминий | 27 | 100 |
| 3 | 14 | Si | Кремний | 28 29 30 |
92,23 4,67 3,10 |
| 3 | 15 | P | Фосфор | 31 | 100 |
| 3 | 16 | S | Сера | 32 33 34 36 |
95,02 0,75 4,21 0,02 |
| 3 | 17 | Cl | Хлор | 35 37 |
75,78 24,22 |
| 3 | 18 | Ar | Аргон | 36 38 40 |
0,337 0,063 99,600 |
| 4 | 19 | K | Калий | 39 41 |
93,258 6,730 |
| 4 | 20 | Ca | Кальций | 40 42 43 44 46 |
96,941 0,647 0,135 2,086 0,004 |
| 4 | 21 | Sc | Скандий | 45 | 100 |
| 4 | 22 | Ti | Титан | 46 47 48 49 50 |
7,95 7,75 73,45 5,51 5,34 |
| 4 | 23 | V | Ванадий | 51 | 99,750 |
| 4 | 24 | Cr | Хром | 50 52 53 54 |
4,345 83,789 9,501 2,365 |
| 4 | 25 | Mn | Марганец | 55 | 100 |
| 4 | 26 | Fe | Железо | 54 56 57 58 |
5,845 91,754 2,119 0,282 |
| 4 | 27 | Co | Кобальт | 59 | 100 |
| 4 | 28 | Ni | Никель | 58 60 61 62 64 |
68,27 26,10 1,13 3,59 0,91 |
| 4 | 29 | Cu | Медь | 63 65 |
69,1 30,9 |
| 4 | 30 | Zn | Цинк | 64 66 67 68 70 |
49,2 27,7 4,0 18,5 0,6 |
| 4 | 31 | Ga | Галлий | 69 71 |
60,11 39,89 |
| 4 | 32 | Ge | Германий | 70 72 73 74 |
20,55 27,37 7,67 36,74 |
| 4 | 33 | As | Мышьяк | 75 | 100 |
| 4 | 34 | Se | Селен | 74 76 77 78 80 |
0,87 9,02 7,58 23,52 49,82 |
| 4 | 35 | Br | Бром | 79 81 |
50,56 49,44 |
| 4 | 36 | Kr | Криптон | 80 82 83 84 86 |
2,28 11,58 11,49 57,00 17,30 |
| 5 | 37 | Rb | Рубидий | 85 | 72,2 |
| 5 | 38 | Sr | Стронций | 84 86 87 88 |
0,56 9,86 7,00 82,58 |
| 5 | 39 | Y | Иттрий | 89 | 100 |
| 5 | 40 | Zr | Цирконий | 90 91 92 94 |
51,46 11,23 17,11 17,4 |
| 5 | 41 | Nb | Ниобий | 93 | 100 |
| 5 | 42 | Mo | Молибден | 92 94 95 96 97 98 |
15,86 9,12 15,70 16,50 9,45 23,75 |
| 5 | 44 | Ru | Рутений | 96 98 99 100 101 102 104 |
5,7 2,2 12,8 12,7 13 31,3 18,3 |
| 5 | 45 | Rh | Родий | 103 | 100 |
| 5 | 46 | Pd | Палладий | 102 104 105 106 108 110 |
1,00 11,14 22,33 27,33 26,46 11,72 |
| 5 | 47 | Ag | Серебро | 107 109 |
51,839 48,161 |
| 5 | 48 | Cd | Кадмий | 106 108 110 111 112 114 |
1,25 0,89 12,47 12,80 24,11 28,75 |
| 5 | 49 | In | Индий | 113 | 4,29 |
| 5 | 50 | Sn | Олово | 112 114 115 116 117 118 119 120 122 124 |
0,96 0,66 0,35 14,30 7,61 24,03 8,58 32,85 4,72 5,94 |
| 5 | 51 | Sb | Сурьма | 121 123 |
57,36 42,64 |
| 5 | 52 | Te | Теллур | 120 122 123 124 125 126 |
0,09 2,55 0,89 4,74 7,07 18,84 |
| 5 | 53 | I | Иод | 127 | 100 |
| 5 | 54 | Xe | Ксенон | 126 128 129 130 131 132 134 |
0,089 1,910 26,401 4,071 21,232 26,909 10,436 |
| 6 | 55 | Cs | Цезий | 133 | 100 |
| 6 | 56 | Ba | Барий | 132 134 135 136 137 138 |
0,10 2,42 6,59 7,85 11,23 71,70 |
| 6 | 57 | La | Лантан | 139 | 99,911 |
| 6 | 58 | Ce | Церий | 136 138 140 142 |
0,185 0,251 88,450 11,114 |
| 6 | 59 | Pr | Празеодим | 141 | 100 |
| 6 | 60 | Nd | Неодим | 142 143 145 146 148 |
27,2 12,2 8,3 17,2 5,7 |
| 6 | 62 | Sm | Самарий | 144 150 152 154 |
3,07 7,38 26,75 22,75 |
| 6 | 63 | Eu | Европий | 151 153 |
52,2 47,8 |
| 6 | 64 | Gd | Гадолиний | 154 155 156 157 158 160 |
2,18 14,80 20,47 15,65 24,84 21,86 |
| 6 | 65 | Tb | Тербий | 159 | 100 |
| 6 | 66 | Dy | Диспрозий | 156 158 160 161 162 163 164 |
0,056 0,095 2,329 18,889 25,475 24,896 28,260 |
| 6 | 67 | Ho | Гольмий | 165 | 100 |
| 6 | 68 | Er | Эрбий | 162 164 166 167 168 170 |
0,139 1,601 33,503 22,869 26,978 14,910 |
| 6 | 69 | Tm | Тулий | 169 | 100 |
| 6 | 70 | Yb | Иттербий | 168 170 171 172 173 174 176 |
0,126 3,023 14,216 21,754 16,098 31,896 12,887 |
| 6 | 71 | Lu | Лютеций | 175 | 97,41 |
| 6 | 72 | Hf | Гафний | 176 177 178 179 180 |
5,26 18,60 27,28 13,62 35,08 |
| 6 | 73 | Ta | Тантал | 181 | 99,9877 |
| 6 | 74 | W | Вольфрам | 182 184 186 |
26,50 30,64 28,43 |
| 6 | 75 | Re | Рений | 185 | 37,07 |
| 6 | 76 | Os | Осмий | 184 187 188 189 190 192 |
0,02 1,96 13,24 16,15 26,26 40,78 |
| 6 | 77 | Ir | Иридий | 191 193 |
37,3 62,7 |
| 6 | 78 | Pt | Платина | 192 194 195 196 198 |
0,782 32,967 33,832 25,242 7,163 |
| 6 | 79 | Au | Золото | 197 | 100 |
| 6 | 80 | Hg | Ртуть | 196 198 199 200 201 202 204 |
0,155 10,04 16,94 23,14 13,17 29,74 6,82 |
| 6 | 81 | Tl | Таллий | 203 205 |
29,52 70,48 |
| 6 | 82 | Pb | Свинец | 204 206 207 208 |
1,4 24,1 22,1 52,4 |
| 6 | 83 | Bi | Висмут | 209[11] | 100 |
Тантал также имеет стабильный изомер (энергетически возбуждённое состояние): 180mTa (изотопная распространённость 0,0123 %).
Кроме стабильных нуклидов, в природных изотопных смесях также присутствуют примордиальные радионуклиды (т. е. нуклиды с очень большими периодами полураспада, сохранившиеся с момента образования Земли).
См. также[править | править код]
- Изобары
- Изотоны
- Изотопная распространённость
- Изомерия атомных ядер
- Таблица нуклидов
- Радиоактивные изотопы
- Изотопический сдвиг
Примечания[править | править код]
- ↑ Isotope. Encyclopedia Britannica. Дата обращения: 24 мая 2019. Архивировано 9 мая 2020 года.
- ↑ Soddy, Frederick The origins of the conceptions of isotopes. Nobelprize.org 393 (12 декабря 1922). — «Thus the chemically identical elements - or isotopes, as I called them for the first time in this letter to Nature, because they occupy the same place in the Periodic Table ...» Дата обращения: 9 января 2019. Архивировано 10 января 2019 года.
- ↑ IUPAC (Connelly, N. G.; Damhus, T.; Hartshorn, R. M.; and Hutton, A. T.), Nomenclature of Inorganic Chemistry — IUPAC Recommendations 2005 Архивная копия от 9 июля 2018 на Wayback Machine, The Royal Society of Chemistry, 2005; IUPAC (McCleverty, J. A.; and Connelly, N. G.), Nomenclature of Inorganic Chemistry II. Recommendations 2000, The Royal Society of Chemistry, 2001; IUPAC (Leigh, G. J.), Nomenclature of Inorganic Chemistry (recommendations 1990), Blackwell Science, 1990; IUPAC, Nomenclature of Inorganic Chemistry, Second Edition Архивная копия от 3 марта 2016 на Wayback Machine, 1970; probably in the 1958 first edition as well
- ↑ Изотопы // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2. (CC BY-SA 3.0)
- ↑ 1 2 Audi G., Kondev F. G., Wang M., Huang W. J., Naimi S. The Nubase2016 evaluation of nuclear properties (англ.) // Chinese Physics C. — 2017. — Vol. 41, iss. 3. — P. 030001-1—030001-138. — doi:10.1088/1674-1137/41/3/030001. — .

- ↑ Soddy, Frederick. Intra-atomic charge (англ.) // Nature. — 1913. — Vol. 92, no. 2301. — P. 399—400. — doi:10.1038/092399c0. — . Архивировано 4 октября 2015 года.
- ↑ IUPAP Red Book Архивная копия от 18 марта 2015 на Wayback Machine // iupap.org.
- ↑ Thoennessen M. (2016). "2015 Update of the Discoveries of Isotopes". arXiv:1606.00456 [nucl-ex].
- ↑ Michael Thoennessen. Discovery of Nuclides Project. Дата обращения: 6 июня 2016. Архивировано 4 марта 2016 года.
- ↑ Петров С. В. Глава 2. Асептика и антисептика // Общая хирургия. — СПб.: Лань, 1999. — С. 672.
- ↑ Практически стабилен, период полураспада 2,01·1019 лет.