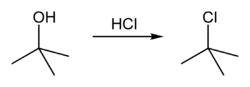
2-метил-2-хлорпропан
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 5 мая 2023 года; проверки требуют 2 правки.
| 2-метил-2-хлорпропан | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
2-метил-2-хлорпропан | ||
| Хим. формула | С4H9Cl | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 92,57 г/моль | ||
| Плотность | 0,851 г/см³ | ||
| Энергия ионизации | 1,7E−18 Дж[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -26 °C | ||
| • кипения | 51 °C | ||
| Структура | |||
| Дипольный момент | 7,1E−30 Кл·м[1] | ||
| Классификация | |||
| Рег. номер CAS | 507-20-0 | ||
| PubChem | 10486 | ||
| Рег. номер EINECS | 208-066-4 | ||
| SMILES | |||
| InChI | |||
| RTECS | TX5040000 | ||
| ChEBI | ChEMBL346997 | ||
| Номер ООН | 1127 | ||
| ChemSpider | 10054 | ||
| Безопасность | |||
| Краткие характер. опасности (H) | 225 | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
2-метил-2-хлорпропан (трет-бутилхлорид) — вещество, состоящее из углерода, водорода и хлора. При нормальных условиях является бесцветной жидкостью, нерастворимой в воде. Легко воспламеняется. Гидролизуется до трет-бутилового спирта. В промышленности используется в качестве прекурсора для синтеза других органических соединений.
Изомеры[править | править код]
2-Метил-2-хлорпропан имеет три изомера: 1-хлорбутан, 2-хлорбутан и 2-метил-1-хлорпропан.
Получение[править | править код]
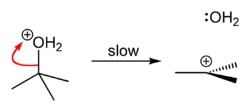
трет-Бутилхлорид получают реакцией трет-бутилового спирта с хлористым водородом. В лаборатории используется концентрированная соляная кислота. Реакция идёт по механизму мономолекулярного нуклеофильного замещения SN1[2].
 |
 |
 |
Общий вид реакции:
Примечания[править | править код]
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ James F. Norris and Alanson W. Olmsted "tert-Butyl Chloride" Org. Synth. 1928, volume 8, pp. 50. doi:10.15227/orgsyn.008.0050