Благородные газы
| Группа → | 18 | ||||||
|---|---|---|---|---|---|---|---|
| ↓ Период | |||||||
| 1 |
| ||||||
| 2 |
| ||||||
| 3 |
| ||||||
| 4 |
| ||||||
| 5 |
| ||||||
| 6 |
| ||||||
| 7 |
| ||||||
Благоро́дные га́зы (также ине́ртные[2] или ре́дкие га́зы[3]) — группа химических элементов со схожими свойствами: при нормальных условиях они представляют собой одноатомные газы без цвета, запаха и вкуса, с очень низкой химической реактивностью. К благородным газам относятся гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радиоактивный радон (Rn). Формально к этой группе также причисляют недавно открытый оганесон (Og), однако его химические свойства почти не исследованы и скорее всего будут близки к свойствам металлоидов, таких как астат (At) и теллур (Te) .
В первых 6 периодах периодической таблицы химических элементов инертные газы относятся к последней, 18-й группе. Согласно старой европейской системе нумерации групп периодической таблицы, группа инертных газов обозначается VIIIA (главная подгруппа VIII-й группы, или подгруппа гелия), согласно старой американской системе — VIIIB; кроме того, в некоторых источниках, особенно в старых, группа инертных газов обозначается цифрой 0, ввиду характерной для них нулевой валентности. Возможно, что из-за релятивистских эффектов элемент 7-го периода 4-й группы флеровий обладает некоторыми свойствами благородных газов[4]. Он может заменить в периодической таблице оганесон[5]. Благородные газы химически неактивны и способны участвовать в химических реакциях лишь при экстремальных условиях.
Характеристики благородных газов объяснены современными теориями структуры атома: их электронные оболочки из валентных электронов являются заполненными, тем самым позволяя участвовать лишь в очень малом количестве химических реакций: известны всего несколько сотен химических соединений этих элементов.
Неон, аргон, криптон и ксенон выделяют из воздуха специальными установками, используя при этом методы сжижения газов и фракционированной конденсации. Источником гелия являются месторождения природного газа с высокой концентрацией гелия, который отделяется с помощью методов криогенного разделения газов. Радон обычно получают как продукт радиоактивного распада радия из растворов соединений этого элемента.
Химические свойства[править | править код]

Благородные газы не поддерживают горения и не возгораются при нормальных условиях.
| № | Элемент | № электронов/электронной оболочки |
|---|---|---|
| 2 | гелий | 2 |
| 10 | неон | 2, 8 |
| 18 | аргон | 2, 8, 8 |
| 36 | криптон | 2, 8, 18, 8 |
| 54 | ксенон | 2, 8, 18, 18, 8 |
| 86 | радон | 2, 8, 18, 32, 18, 8 |
| 118 | оганесон | 2, 8, 18, 32, 32, 18, 8 |
Соединения[править | править код]
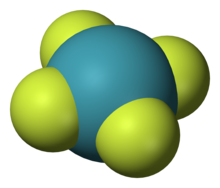
Инертные газы отличаются химической неактивностью (отсюда и название). Тем не менее, в 1962 году Нил Барлетт показал, что все они при определённых условиях могут образовывать соединения (особенно охотно со фтором). Наиболее «инертны» неон и гелий: чтобы заставить их вступить в реакцию, нужно применить много усилий, искусственно ионизируя каждый атом. Ксенон же, наоборот, слишком активен (для инертных газов) и реагирует даже при нормальных условиях, демонстрируя чуть ли не все возможные степени окисления (+1, +2, +4, +6, +8). Радон тоже имеет высокую химическую активность (по сравнению с лёгкими инертными газами), но он радиоактивен и быстро распадается, поэтому подробное изучение его химических свойств осложнено, в отличие от ксенона.
Оганесон, несмотря на его принадлежность к 18-й группе периодической таблицы, может не являться инертным газом, так как предполагается, что при нормальных условиях в силу релятивистских эффектов, влияющих на движение электронов вблизи его ядра с высоким зарядом, он будет находиться в твёрдом состоянии[6].
Физические свойства[править | править код]

Инертные газы бесцветны, прозрачны и не имеют запаха и вкуса. В небольшом количестве они присутствуют в воздухе и некоторых горных породах, а также в атмосферах некоторых планет-гигантов и планет земной группы. Гелий является вторым (после водорода) по распространённости элементом во Вселенной, однако для Земли он является редким газом, который улетучился в космос во время образования планеты. Почти весь добываемый гелий является радиогенным продуктом происходящего в течение миллиардов лет в недрах Земли альфа-распада урана, тория и их дочерних элементов; лишь малая часть земного гелия сохранилась от эпохи образования Солнечной системы. Аналогично, по большей части радиогенным является и аргон, возникший в результате постепенного радиоактивного распада калия-40.
При нормальных условиях все элементы 18-й группы (кроме, возможно, оганесона) являются одноатомными газами. Их плотность растёт с увеличением номера периода. Плотность гелия при нормальных условиях примерно в 7 раз меньше плотности воздуха, тогда как радон почти в восемь раз тяжелее воздуха.
При нормальном давлении температуры плавления и кипения у любого благородного газа отличаются менее чем на 10 °C; таким образом, они остаются жидкими лишь в малом температурном интервале. Температуры сжижения и кристаллизации растут с ростом номера периода. Гелий под атмосферным давлением вообще не становится твёрдым даже при абсолютном нуле — единственный из всех веществ.
Биологическое действие[править | править код]
Инертные газы не обладают химической токсичностью. Однако атмосфера с увеличенной концентрацией инертных газов и соответствующим снижением концентрации кислорода может оказывать удушающее действие на человека, вплоть до потери сознания и смерти[7][8]. Известны случаи гибели людей при утечках инертных газов.
Ввиду высокой радиоактивности всех изотопов радона он является радиотоксичным. Наличие радона и радиоактивных продуктов его распада во вдыхаемом воздухе вызывает стохастические эффекты хронического облучения, в частности рак.
Инертные газы обладают биологическим действием, которое проявляется в их наркотическом воздействии на организм и по силе этого воздействия располагаются по убыванию в следующем порядке (в сравнении приведены также азот и водород): Xe — Kr — Ar — N2 — H2 — Ne — He. При этом ксенон и криптон проявляют наркотический эффект при нормальном барометрическом давлении, аргон — при давлении свыше 0,2 МПа (2 атм), азот — свыше 0,6 МПа (6 атм), водород — свыше 2,0 МПа (20 атм). Наркотическое действие неона и гелия в опытах не регистрируются, так как под давлением раньше возникают симптомы «нервного синдрома высокого давления» (НСВД)[9].
Применение[править | править код]

Лёгкие инертные газы имеют очень низкие точки кипения и плавления, что позволяет их использовать в качестве холодильного агента в криогенной технике. Жидкий гелий, который кипит при 4,2 К (−268,95 °C), используется для получения сверхпроводимости — в частности, для охлаждения сверхпроводящих обмоток электромагнитов, применяемых, например, для магнитно-резонансной томографии и других приложений ядерного магнитного резонанса. Жидкий неон, хотя его температура кипения (–246,03 °C) и не достигает таких низких значений как у жидкого гелия, также находит применение в криогенике, потому что его охлаждающие свойства (удельная теплота испарения) более чем в 40 раз лучше, чем у жидкого гелия, и более чем в три раза лучше, чем у жидкого водорода.
Гелий, благодаря его пониженной растворимости в жидкостях, особенно в липидах, используется вместо азота как компонент дыхательных смесей для дыхания под давлением (например, при подводном плавании). Растворимость газов в крови и биологических тканях растёт под давлением. В случае использования для дыхания обычного воздуха или других азотсодержащих дыхательных смесей это может стать причиной эффекта, известного как азотное отравление.
Благодаря меньшей растворимости в липидах, атомы гелия задерживаются клеточной мембраной, и поэтому гелий используется в дыхательных смесях, таких как тримикс и гелиокс, уменьшая наркотический эффект газов, возникающий на глубине. Кроме того, пониженная растворимость гелия в жидкостях тела позволяет избежать кессонной болезни при быстром всплытии с глубины. Уменьшение остатка растворённого газа в теле означает, что во время всплытия образуется меньшее количество газовых пузырьков; это уменьшает риск газовой эмболии. Другой инертный газ, аргон, рассматривается как лучший выбор для использования в качестве прослойки к сухому костюму[10][неавторитетный источник] для подводного плавания.
Аргон, наиболее дешёвый среди инертных газов (его содержание в атмосфере составляет около 1 %), широко используется при сварке в защитных газах, резке и других приложениях для изоляции от воздуха металлов, реагирующих при нагреве с кислородом (и азотом), а также для обработки жидкой стали. Аргон также применяется в люминесцентных лампах для предотвращения окисления разогретого вольфрамового электрода. Также, ввиду низкой теплопроводности, аргон (а также криптон) используют для заполнения стеклопакетов.
После крушения дирижабля «Гинденбург» в 1937 году огнеопасный водород был заменен негорючим гелием в качестве заполняющего газа в дирижаблях и воздушных шарах, несмотря на снижение плавучести на 8,6 % по сравнению с водородом. Несмотря на замену, катастрофа оказала непропорционально большое влияние на всю область герметичных летательных аппаратов легче воздуха и подорвала планы по расширению этой области авиации более чем на полвека. Они стали популярнее только в последнее время, с развитием нановолоконных тканей и альтернативной энергетики.
Цвета и спектры благородных газов[править | править код]
| Форма | Гелий | Неон | Аргон | Криптон | Ксенон |
| В колбе под действием электричества | 
|

|

|

|

|
| В прямой трубке | 
|

|

|

|

|
| В трубках-литерах Периодической таблицы | 
|

|

|

|

|
| Cпектр поглощения газа |
См. также[править | править код]
Примечания[править | править код]
- ↑ Meija J., Coplen T. B., Berglund M., Bièvre P. D., Gröning M., Holden N. E., Irrgeher J., Loss R. D., Walczyk T., Prohaska T. Atomic weights of the elements 2005 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry — IUPAC, 2016. — Vol. 88, Iss. 3. — ISSN 0033-4545; 1365-3075; 0074-3925 — doi:10.1515/PAC-2015-0305
- ↑ Инертные газы // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2. (CC BY-SA 3.0)
- ↑ Благородные газы — статья из Химической энциклопедии
- ↑ Flerov laboratory of nuclear reactions. JINR. Дата обращения: 8 августа 2009. Архивировано 6 октября 2011 года.
- ↑ Nash, Clinton S. Atomic and Molecular Properties of Elements 112, 114, and 118 (англ.) // J. Phys. Chem. A : journal. — 2005. — Vol. 109, no. 15. — P. 3493—3500. — doi:10.1021/jp050736o. — PMID 16833687.
- ↑ Wieser M. E. Atomic weights of the elements 2005 (IUPAC Technical Report) (англ.) // Pure Appl. Chem. : journal. — 2006. — Vol. 78, no. 11. — P. 2051—2066. — doi:10.1351/pac200678112051.
- ↑ Опасности при работе с азотом и аргоном. Дата обращения: 31 марта 2011. Архивировано 16 октября 2014 года.
- ↑ Инструкция по эксплуатации баллонов с аргоном, используемых в спектральной лаборатории. Дата обращения: 31 марта 2011. Архивировано из оригинала 25 июля 2010 года.
- ↑ Павлов Б. Н. Проблема защиты человека в экстремальных условиях гипербарической среды обитания. www.argonavt.com (15 мая 2007). Дата обращения: 22 мая 2010. Архивировано 22 августа 2011 года.
- ↑ en:Dry_suit (англ.)
Литература[править | править код]
- Беннетт, Питер; Эллиотт, Дэвид. The Physiology and Medicine of Diving (англ.). — SPCK Publishing, 1998. — ISBN 0-7020-2410-4.
- Bobrow Test Preparation Services. CliffsAP Chemistry (англ.). — CliffsNotes, 2007. — ISBN 0-470-13500-X.
- Гринвуд, Н. Н.; Ёрншо, A. Chemistry of the Elements (англ.). — 2nd. — Oxford:Butterworth-Heinemann, 1997. — ISBN 0-7506-3365-4.
- Хардинг, Чарли Дж.; Джейнс, Роб. Elements of the P Block (англ.). — Royal Society of Chemistry, 2002. — ISBN 0-85404-690-9.
- Холловэй, Джон. Noble-Gas Chemistry (англ.). — Лондон: Methuen Publishing, 1968. — ISBN 0-412-21100-9.
- Менделеев, Дмитрий Основы Химии. — 7-е.
- Оджима, Минору; Подосек, Франк. Noble Gas Geochemistry (англ.). — Cambridge University Press, 2002. — ISBN 0-521-80366-7.
- Вайнхольд, Ф.; Лэндис, C. Valency and bonding (англ.). — Cambridge University Press, 2005. — ISBN 0-521-83128-8.
- Скерри, Эрик. The Periodic Table, Its Story and Its Significance (англ.). — Oxford University Press, 2007. — ISBN 0-19-530573-6.
Ссылки[править | править код]
В статье есть список источников, но не хватает сносок. |