Лиганд
Лига́нд (от лат. ligare «связывать») — атом, ион или молекула, связанные с другим атомом (акцептором) с помощью донорно-акцепторного взаимодействия. Понятие применяется в химии комплексных соединений, обозначая присоединенные к одному или нескольким центральным (комплексообразующим) атомам металла частицы.
Чаще всего такое связывание происходит с образованием так называемой «координационной» донорно-акцепторной связи, где лиганды выступают в роли основания Льюиса, то есть являются донорами электронной пары. При присоединении лигандов к центральному атому химические свойства комплексообразователя и самих лигандов часто претерпевают значительные изменения.
Номенклатура лигандов[править | править код]
- Первым в названии соединения в именительном падеже называется анион, а затем в родительном — катион.
- В названии комплексного иона сначала перечисляются лиганды в алфавитном порядке, а затем центральный атом.
- Центральный атом в нейтральных катионных комплексах называются русским названием, а в анионах корнем латинского названия с суффиксом «ат». После названия центрального атома указывается степень окисления.
- Число лигандов, присоединённых к центральному атому, указывается приставками моно-, ди-, три-, тетра-, пента-, и т. д.
Характеристики лигандов[править | править код]
Электронное строение[править | править код]
Собственно, важнейшая характеристика лиганда, позволяющая оценить и спрогнозировать его способности к комплексообразованию и саморазрушению D-орбитали — разрушения соединения в целом. В первом приближении включает в себя количество электронных пар, которые лиганд способен выделить на создание координационных связей и электроотрицательность донирующего атома или функциональной группы.
Дентатность[править | править код]

Число занимаемых лигандом координационных мест центрального атома (или атомов) называется дентатностью (от лат. dens, dent- — зуб). Лиганды, занимающие одно координационное место, называются монодентатными (например, NH3), два — бидентатными (оксалат-анион [O-C(=O)-C(=O)-O]2−). Лиганды, способные занять большее количество позиций в координационной сфере, обычно обозначают как полидентатные. Например, этилендиаминтетрауксусная кислота (EDTA), способная занять шесть координационных позиций.
Кроме дентатности, существует характеристика, отражающая количество атомов лиганда, связанных с одним координационным местом центрального атома. В английской литературе обозначается словом hapticity и имеет номенклатурное обозначение η с соответствующим надстрочным индексом. Хотя устоявшегося термина в русском языке она, по-видимому, не имеет, в некоторых источниках можно встретить кальку «гаптность»[1]. Как пример, можно привести циклопентадиенильный лиганд в металлоцентровых комплексах, занимающий одно координационное место (то есть являющийся монодентатным) и связанный через все пять атомов углерода: η5-[C5H5]−.
Способы координации[править | править код]
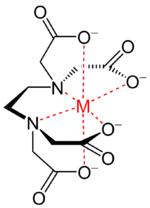
Лиганды с дентатностью больше двух способны образовывать хелатные комплексы (греч. χηλή — клешня) — комплексы, где центральный атом включён в один или более циклов с молекулой лиганда. Такие лиганды называются хелатирующими. Как пример можно привести комплексы тетрааниона той же EDTA, обратив внимание, что несколько из четырёх связей M—O в нём могут формально являться ионными.
При образовании хелатных комплексов часто наблюдается хелатный эффект — большая их стабильность по сравнению с аналогичными комплексами не-хелатирующих лигандов. Он достигается за счёт большего экранирования центрального атома от замещающих воздействий и энтропийного эффекта. Например, константа диссоциации аммиачного комплекса кадмия [Cd(NH3)4]2+ почти в 1500 раз больше, чем комплекса с этилендиамином [Cd(en)2]2+. Причина этого заключается в том, что при взаимодействии гидратированного иона кадмия(II) с этилендиамином две молекулы лиганда вытесняют четыре молекулы воды. При этом число свободных частиц в системе значительно возрастает, и энтропия системы возрастает (а внутренняя упорядоченность комплекса соответственно растёт). То есть причина хелатного эффекта — увеличение энтропии системы при замещении монодентатных лигандов полидентатнымии и, как следствие, снижение энергии Гиббса[2].

Среди хелатирующих лигандов можно выделить класс макроциклических лигандов — молекул с достаточным для помещения атома комплексообразователя размером внутрициклического пространства. Примером таких соединений могут служить порфириновые основания — основы важнейших биохимических комплексов, таких, как гемоглобин, хлорофилл и бактериохлорофилл. Также в качестве макроциклических лигандов могут выступать краун-эфиры, каликсарены и др.
Лиганды также могут являться мостиковыми, образуя связи между различными центральными атомами в би- или полиядерных комплексах. Мостиковые лиганды обозначаются греческой буквой μ (мю).
Примечания[править | править код]
- ↑ Реутов О. А., Курц А. Л., Бутин К. П. Органическая химия. В 4-х частях. Часть 4. — М.: БИНОМ. Лаборатория знаний, 2004. — 726 с. — ISBN 5-94774-113-X.
- ↑ Г. П. Жмурко, Е. Ф. Казакова, В. Н. Кузнецов, А. В. Ященко «Общая химия» под редакцией профессора С. Ф. Дунаева, Академия, 2011. — 240 с.
Литература[править | править код]
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2 (Даф-Мед). — 671 с. — ISBN 5-82270-035-5.