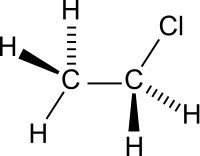
Хлорэтан
| Хлорэтан | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Хлорэтан |
| Традиционные названия | монохлорэтан, этилхлорид, хлористый этил |
| Хим. формула | C2H5Cl |
| Физические свойства | |
| Состояние | газ |
| Молярная масса | 64,51 г/моль |
| Плотность | 0,8898 г/см³ |
| Энергия ионизации | 10,97 ± 0,01 эВ[1][2] |
| Термические свойства | |
| Температура | |
| • плавления | −138,7 °C |
| • кипения | 12,27 °C |
| • вспышки | −58 ± 1 ℉[1] |
| Пределы взрываемости | 3,8 ± 0,1 об.%[1] |
| Давление пара | 1000 ± 1 мм рт.ст.[1] |
| Структура | |
| Дипольный момент | 6,8E−30 Кл·м[2] |
| Классификация | |
| Рег. номер CAS | 75-00-3 |
| PubChem | 6337 |
| Рег. номер EINECS | 200-830-5 |
| SMILES | |
| InChI | |
| RTECS | KH7525000 |
| ChEBI | 47554 |
| ChemSpider | 6097 |
| Безопасность | |
| Токсичность | ядовит, огнеопасен, канцероген |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Хлорэтан | |
|---|---|
 | |
 | |
 | |
| Химическое соединение | |
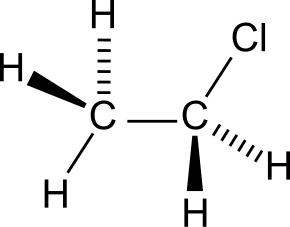
| Брутто-формула | C2H5Cl |
| CAS | 75-00-3 |
| PubChem | 6337 |
| DrugBank | 13259 |
| Состав | |
| Классификация | |
| АТХ | N01BX01 |
| Другие названия | |
| хлористый этил, этилхлорид | |
Хлорэта́н (хлорэтил, этилхлорид, хлористый этил, лат. Aethylii chloridum) — хлорорганическое вещество, однозамещённый галогеналкан с формулой C2H5Cl. Бесцветный легкосжижаемый газ со слабым характерным запахом, огнеопасен. Применяется в медицине для анестезии методом сильного охлаждения, ранее иногда использовался для ингаляционного наркоза, и применяется в рекреационных целях, наподобие попперс и закиси азота.
Впервые был получен алхимиком Василием Валентином в 1440 году в реакции этилового спирта и соляной кислоты[3]
Также известен как хладагент R-160.
Синонимы[править | править код]

Этилхлорид, Aether chloratus, Aethylis chloridum, Aethylium chloratum, Chelen, Chlorene, Chloretan, Ethylis chloridum, Ethyl chloride, Kelen, Хлористый этил, хлорэтан.
Общая информация[править | править код]
Хлорэтил является мощным наркотическим средством. При концентрации хлорэтила во вдыхаемой смеси 3—4 об. % наступает хирургическая стадия наркоза. Наркоз развивается быстро, в течение 2—3 мин, стадия возбуждения непродолжительна. Пробуждение наступает быстро.
Основной недостаток хлорэтила — малая терапевтическая широта и в связи с этим опасность передозировки.
В настоящее время хлорэтил применяют для наркоза редко (лишь при очень кратковременных оперативных вмешательствах), в основном он используется как местное средство для кратковременного поверхностного обезболивания кожных покровов.
При попадании на кожу он вызывает вследствие быстрого испарения сильное охлаждение кожи, ишемию и понижение чувствительности, что позволяет пользоваться им при небольших поверхностных операциях (разрезы кожи).
Кроме того, хлорэтилом пользуются для уменьшения кожного зуда, а также для лечения (криотерапия) рожистого воспаления, нейромиозитов, невралгий, термических ожогов, бородавчатой формы красного лишая, очаговой алопеции. Для этих целей с бокового капилляра ампулы с хлорэтилом снимают резиновый колпачок, согревают ампулу в ладони и выделяющуюся струю направляют на поверхность кожи (с расстояния 25—30 см). После появления на коже «инея» ткани становятся плотными и нечувствительными. В лечебных целях процедуры производят раз в день в течение 7—10 дней.
Применять хлорэтил следует с осторожностью: возможны гиперемия и повреждение целостности кожи с экссудацией.
Противопоказания[править | править код]
Противопоказаниями к применению являются нарушения целостности кожных покровов, заболевания сосудов (варикозное расширение вен, сосудистые спазмы). Больные не должны вдыхать хлорэтил, испаряющийся с поверхности кожи.
Физические свойства[править | править код]
Прозрачная, бесцветная, легко летучая жидкость своеобразного запаха. Трудно растворим в воде (приблизительно 1:50). Смешивается во всех соотношениях со спиртом и эфиром. Огнеопасен. Горит, окрашивая пламя в зелёный цвет. Плотность 0,919—0,923 (при 0 °C). Температура кипения +12—13°С.
Форма выпуска[править | править код]
- в ампулах по 30 мл в упаковке по 10 штук.
Хранение[править | править код]
В прохладном, защищённом от света месте.
Литература[править | править код]
- Менделеев Д. И., Сум Н.,. Этил хлористый // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Примечания[править | править код]
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0267.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Rossberg M. et al. Chlorinated Hydrocarbons // Ullmann's Encyclopedia of Industrial Chemistry (англ.). — Weinheim: Wiley-VCH, 2006. — doi:10.1002/14356007.a06_233.pub2.
Это заготовка статьи по фармакологии. Помогите Википедии, дополнив её. |
